研究课题Title:蛋白纯化及检测报告
学校班级School/Class:徐州市撷秀中学 高一(24)班
小组成员Names:齐潇然 王远博
指导教师Teacher:王佳佳 满卫萍
研究背景Background:蛋白质在科学研究具有中极其重要的作用,贯穿了生命科学,医学、化学、材料科学乃至基因工程等多个领域。科学实验需要干扰素伽玛,我们通过编辑基因片段植入大肠杆菌用于生产目标蛋白并纯化,此实验旨在检测生产出的干扰素伽玛是否符合要求标准。
目的与意义Purpose:在蛋白质纯化过程中,了解目标蛋白的等电点,疏水性,大小等特性,增进对蛋白质本身的理解。通过对蛋白质进行纯化及检测,保证其纯度,结构完整性和功能活性,为其他以此为原料的科研项目和工业生产奠定基础。
概述Overview:蛋白质的分离,提纯与鉴定是生物化学与分子生物学研究的基础。高效的纯化策略,旨在从复杂混合物中获得高纯度具有生物活性的目标蛋白,并对其进行准确鉴定。
本课题的核心流程通常包括细胞裂解,粗分级与精细纯化。首先通过超声没解或者去皱剂等方法,破损细胞释放内容物测温经常利用硫酸铵沉淀等快速浓缩目标蛋白,精细纯化则主要依赖柱层析技术,亲和层析利用标签与固定化酶特性结合,实现一步高效纯化;交换层析和尺寸排组层析则分别依据电荷与分子大小进行分离,能进一步提高纯度。
过程需要全程监控。SDS-聚丙烯胺凝胶电泳(SDS-PAGE)最常用的纯度与分子量分析工具。Western Blot利用抗原-抗体反应,可特异性鉴定目标蛋白,最终通过比色法或紫外吸收法定量蛋白浓度,并通过功能实验验证其生物活性。
综上,整合多种层析技术与检测手段,是获得高质量蛋白的制品服务于下游结构与功能研究的关键。
实验材料与方法(一)——目的蛋白的纯化
实验材料:亲和层析填料、EP管、50毫升离心管、纯化缓冲溶液,G250溶液、裂解缓冲液、平衡缓冲液、洗涤缓冲液(20毫摩尔咪唑)、洗脱缓冲液1(50毫摩尔的咪唑)、洗脱缓冲液2(100毫摩尔咪唑)、洗脱缓冲液3(500毫摩尔的咪唑)。
使用超声破碎仪对表达菌体进行裂解,离心收集含有目标蛋白的上清液。
![]() 01.样品处理:
01.样品处理:
使用超声破碎仪对表达菌体进行裂解,离心收集含有目标蛋白的上清液。
![]() 02.纯化
02.纯化
• 平衡: 将亲和层析填料装入重力柱,用平衡液冲洗5-10个柱体积。
• 上样:将样品上清加入平衡好的柱子
• 洗杂:洗去非特异性结合蛋白
• 洗脱:咪唑梯度洗脱目标蛋白。
![]() 03. 检测与透析
03. 检测与透析
SDS-PAGE电泳初步鉴定纯化效果,透析去除咪唑。
实验材料与方法(二)——目的蛋白的浓度检测
实验材料:EP管、酶标板、10ul&300ul枪头、Bradford检测试剂盒、透析溶液
![]() 01. 标品配置
01. 标品配置
配制0、0.125、0.25、0.5、0.75、1、1.5mg/ml蛋白标准。
![]() 02. 检测:将标准品和样品与Bradford试剂混合,用酶标仪测定A595。可测定吸光度。
02. 检测:将标准品和样品与Bradford试剂混合,用酶标仪测定A595。可测定吸光度。
![]() 03. 计算浓度:使用exccl表格中工具制定浓度为x轴,吸光值为y轴的拟合线性曲线,再将样品吸光值带入到曲线中,计算得到蛋白浓度。
03. 计算浓度:使用exccl表格中工具制定浓度为x轴,吸光值为y轴的拟合线性曲线,再将样品吸光值带入到曲线中,计算得到蛋白浓度。
实验材料与方法(三)—— Western Blot检测
实验材料:12%SDS-PAGE胶,离心管,小型摇床,10ul枪头、10XTris 缓冲液、1XTBST、10X电泳缓冲液、1X电泳液、10X湿转缓冲液、转膜液、 Westem blot封闭液(5%脱脂牛奶)、二抗稀释液
01. SDS-PAGE
通过电泳技术将蛋白质样品按分子量大小进行分离。
02. 转膜
利用电转印技术将凝胶中的蛋白质转移到PVDF膜上
03. 封闭
转膜完毕后,用5%脱脂牛奶封闭膜上非特异性结合,放置室温摇床~60min。
04. 一抗孵育
封闭结束,孵育相应一抗,室温孵育1-2h,孵育完成后加入1XTBST 室温摇床洗膜3遍,每遍5min。
05. 二抗孵育
孵育对应二抗,放置室温摇床孵育1~2h,加入1XTBST室温摇床洗膜3遍,每遍5min。
06. 结果曝光
按 1:1 比例混合ECL化学发光液中A液和B液,均匀涂抹在膜上,使用曝光成像仪显像。
实验结果与分析(一)——SDS-PAGE结果
实验结论分析
上清:与目标蛋白结合
流穿:与目标蛋白结合
洗杂:与杂质蛋白结合
浓度20咪唑:浓度不足以把目标蛋白提纯
浓度50咪唑:浓度不足以把目标蛋白提纯[1]
浓度100咪唑:浓度足够提纯目标蛋白
浓度500咪唑:浓度足够提纯目标蛋白
(注:上清指的是工程菌经裂解液重悬、超声破碎后,经 12000rpm、4℃离心 30 分钟,离心管中形成的上层澄清液体)
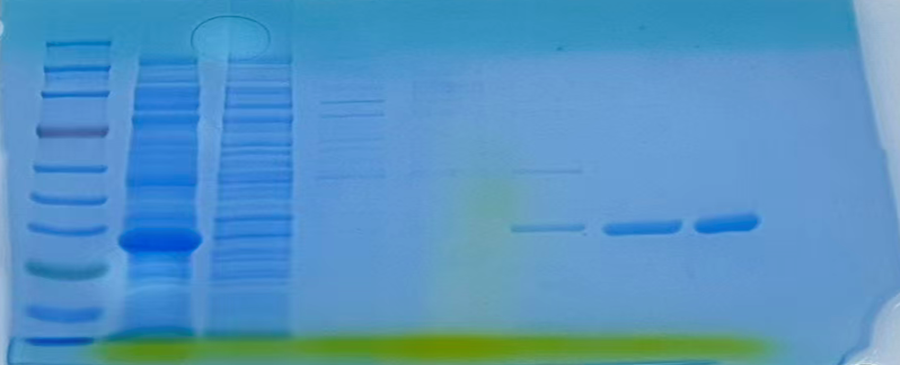 图1:目标蛋白SDS-PAGE电泳检测图谱
图1:目标蛋白SDS-PAGE电泳检测图谱
实验结果与分析(二)—— 蛋白浓度结果
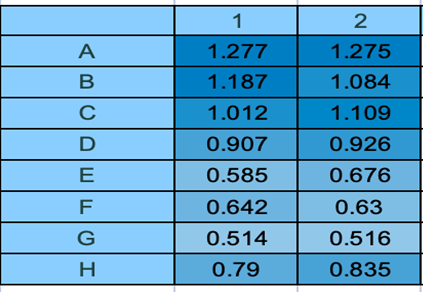
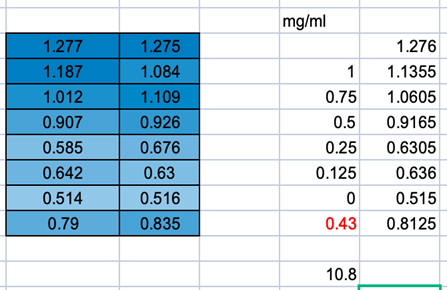
蛋白浓度测定 (Bradford法)
标准曲线拟合分析
基于标准品吸光度值绘制标准曲线,线性相关系数 R² =0.9627,表明标准曲线拟合度良好,可用于定量计算。
目标蛋白浓度计算结果
纯化后蛋白浓度:10.8 mg/ml
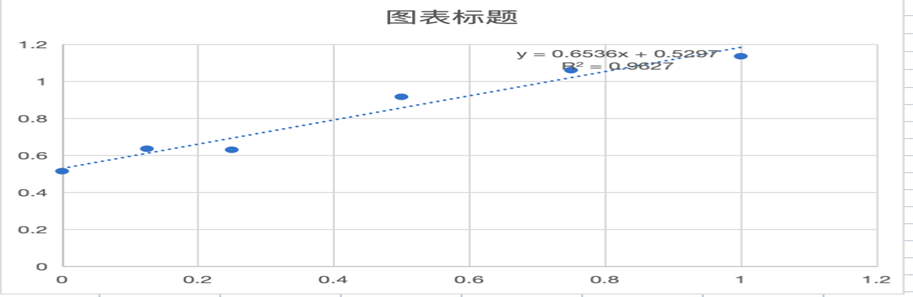 图2:吸光度值随目标蛋白浓度变化曲线图
图2:吸光度值随目标蛋白浓度变化曲线图
|
|
实验结果与分析(二)——蛋白浓度与Western Blot结果
Western Blot特异性鉴定
结果分析:
在预期的分子量位置出现了清晰的特异性条带,无明显杂带,证实了目标蛋白的成功表达与纯化。
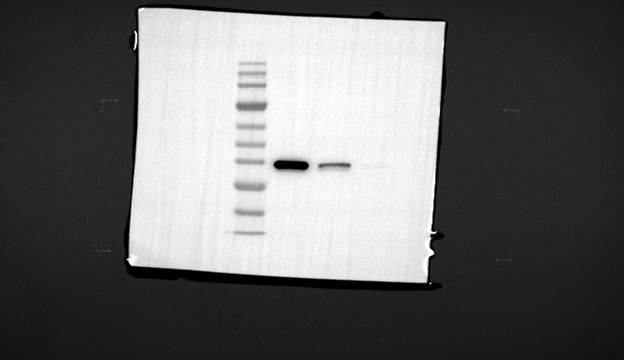
图3 Western Blot特异性鉴定
结论与展望
【实验结论】
·蛋白质成功表达
·目标蛋白纯化成功
·目标蛋白高纯度
·蛋白完整、无明显降解
本实验通过诱导表达、破碎、亲和层析等步骤,成功纯化获得高纯度的目标蛋白,其分子量与理论值相符,且具有预期的生物活性,可用于后续结构分析或功能研究。
【未来展望】
→进一步优化纯化条件(如pH值、洗脱液浓度),以提高蛋白的产量和纯度,降低生产成本。
→蛋白易降解
→表达量低
→将纯化后的蛋白用于后续的功能研究、晶体结构解析,或作为靶点进行药物筛选。
